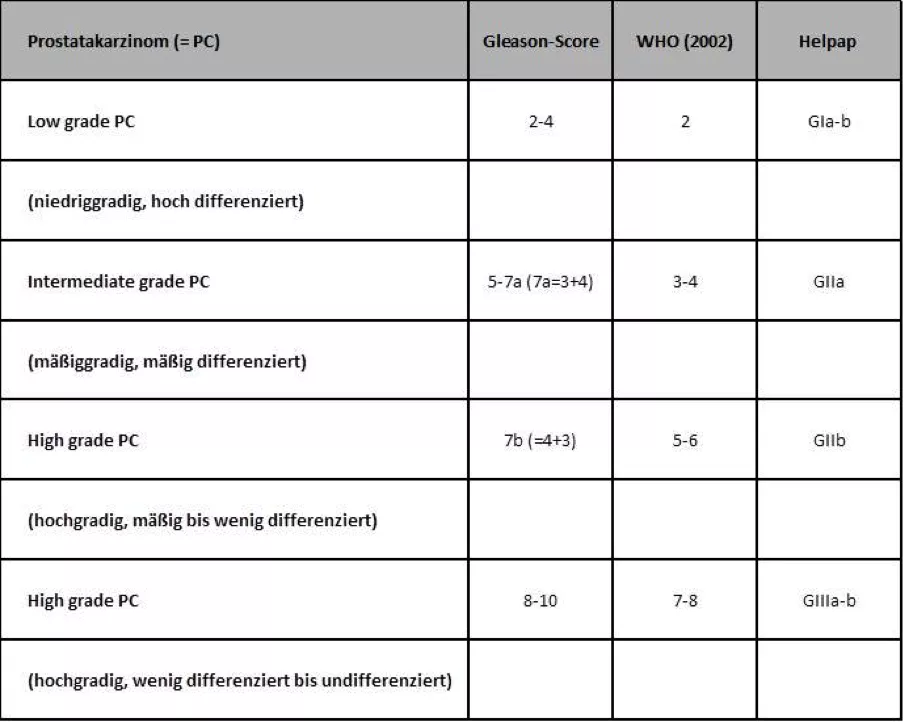
Klassifikation des Prostatakarzinoms
Die Bestimmung des Tumor-Typs (Typing) ergibt in den meisten Fällen ein Adenokarzinom (Drüsenzell-Krebs). Dessen Malignität (Bösartigkeit) wird eingestuft (Grading) und als Gleason-Score ausgewiesen.
Damit der Arzt die richtige Behandlung auswählen und eine korrekte Prognose abgeben kann, muss der Tumor klassifiziert werden. Denn die verschiedenen Tumoren zeigen ein höchst unterschiedliches Verhalten in Wachstum und Ausbreitung.
Zur Klassifikation arbeitet ein Pathologe das aus der Prostata entnommene Gewebe auf und untersucht es mikroskopisch, gegebenenfalls auch mit weiteren histologischen (feingeweblichen) Untersuchungs-Verfahren (immunhistochemische Untersuchungen). Das Gewebe kann aus einer Biopsie stammen (s. Untersuchung) oder aus einer Operation (z.B. radikale Prostatektomie, TUR-P = transurethrale Resektion der Prostata). Wichtig für die Beurteilung sind der Aufbau des Gewebes (Histologie) und das Aussehen der Zellen (Zytologie).
Typing: Bestimmung des Tumor-Typs
Nach der WHO-Klassifikation (WHO = World Health Organization, Weltgesundheitsorganisation) unterscheidet man gutartige Tumoren und Krebsvorstufen von den bösartigen Tumoren der Prostata (s. Prostatakrebs). Zu den ersten beiden Gruppen gehören:
- AAH (atypische adenomatöse Hyperplasie): Verdächtiges Gewebe
- ASAP (engl. atypical small acinar proliferation = atypische mikroazinäre Proliferation): krebsverdächtiges Gewebe
- LG-PIN (engl. low grade PIN = geringgradige prostatische intraepitheliale Neoplasie): Harmlose Veränderung
- HG-PIN (engl. high grade PIN = hochgradige prostatische intraepitheliale Neoplasie): Mögliche Krebsvorstufe (Präkanzerose)
Die bösartigen Tumoren werden nach ihrem Ursprung weiter eingeteilt in:
- Epitheliale Tumoren (am häufigsten): Sie gehen von Epithelzellen (Oberflächenzellen, darunter auch Drüsenzellen) aus und werden deshalb als Prostatakarzinom bezeichnet (Näheres s. u.).
- Sarkome (sehr selten): Sie entstehen aus Zellen des Zwischengewebes der Prostata (z. B. Muskelzellen, Bindegewebe).
- Sekundäre Tumoren (sehr selten): Sie wachsen aus der Nachbarschaft in die Prostata ein oder sind Metastasen (Tochtergeschwülste) von bösartigen Tumoren an anderen Stellen des Körpers.
Mindestens 90% aller Prostatakarzinome entstehen vorwiegend aus Drüsenzellen und werden deshalb Adenokarzinome genannt. Die seltenen restlichen Prostatakarzinome können sich auch von anderen Epithelzellen ableiten.
Grading: Einstufung des Malignitätsgrades
Die Malignität (Bösartigkeit) des Prostatakarzinoms hängt vom Tumor-Typ ab und davon, wie stark sich Gewebearchitektur und Zellen vom normalen Ursprungsgewebe der Prostata unterscheiden: Bei geringen Abweichungen spricht man von einem hoch differenzierten (= wenig entdifferenzierten) Tumor, bei starken Abweichungen von einem schlecht differenzierten (= stark entdifferenzierten) Tumor.
Die Malignität und damit Aggressivität des Tumors steigt mit seiner Entdifferenzierung. Diese zeigt sich an unregelmäßigen Zellen und einem ungeordneten Wachstumsmuster (z.B. kribriform = siebförmig). Mikroskopisch und darüber hinaus mit verschiedenen Spezialverfahren zur feingeweblichen Untersuchung durch den Pathologen lassen sich somit zahlreiche Unterformen des Prostatakarzinoms voneinander abgrenzen.
Ziel des Grading (von engl. to grade = abstufen) ist, die Unterschiede zwischen Karzinom und normalem Gewebe exakt zu erfassen und damit den Malignitätsgrad (das Ausmaß der Bösartigkeit) zu bestimmen. Hierzu wurden diverse Einteilungen („Grading-Systeme“) entwickelt. Außer dem TNM-Grading gelten sie nur für Adenokarzinome und berücksichtigen Gewebemuster und Zell-Befunde in unterschiedlichem Ausmaß:
TNM-Grading: Das TNM-System (s. Wachstum und Ausbreitung) beinhaltet weiterhin eine Einteilung in hoch (G1), mäßig (G2) und schlecht (G3-4) differenzierte Prostatakarzinome.
Gleason-Score: Die Einteilung nach Gleason ist am weitesten verbreitet und soll bei allen gewöhnlichen Prostatakarzinomen angewendet werden. Darin sind fünf verschiedene Wachstumsmuster genau beschrieben und nach steigender Abweichung vom normalen Gewebe von 1 (= gering) bis 5 (= stark) bewertet (s. Abb.). Die Vergabe der Punktzahl (engl. score) geschieht getrennt für das primäre (vorherrschende) und das sekundäre (weitere) Muster. Im Gleason-Score werden dann die Summe und die Einzelwertungen angegeben: Zum Beispiel Muster 2 plus Muster 3 gleich Gleason-Score 5, abgekürzt 5(2+3). Der niedrigste Malignitätsgrad hat demnach einen Gleason-Score von 2(1+1), der höchste einen von 10(5+5).
Abbildung: Die fünf Wachstumsmuster des Adenokarzinoms der Prostata nach dem modifizierten Gleason-Grading von 2005 (schematisiert nach D. F. Gleason, Human Pathology 1992 3: 273-279, J. I. Epstein et al., Am. J. Surg. Pathol. 2005 29: 1228-1242, und B. Helpap et al., Urologe 2007 46: 59-62)
Für die Diagnostik des Gleason-Scores wurde zur internationalen Konsensus-Konferenz der Uropathologen ein neues Graduierungssystem akzeptiert und beschlossen. Es basiert auf dem Gleason-System und unterscheidet 5 Graduierungsgruppen (1-5):
| Graduierungsgruppe 1 | Gleason-Score 3+3=6 |
| Graduierungsgruppe 2 | Gleason-Score 3+4=7 |
| Graduierungsgruppe 3 | Gleason-Score 4+3=7 |
| Graduierungsgruppe 4 | Gleason-Score 4+4=8 Gleason-Score 3+5=8 Gleason-Score 5+3=8 |
| Graduierungsgruppe 5 | Gleason-Score 9-10 |
Der Gleason-Score 2-5 wird damit praktisch nicht mehr verwendet. So wird bei einem Tumor der Graduierungsgruppe 1 inzwischen in den meisten Fällen die aktive Überwachung (active surveillance) angestrebt.
Die neue Klassifikation erlaubt somit eine genaue und damit präzise Stratifikation des Tumors.
Epstein, J.I.; Feng, Z.; Trock, B. J. et al. (2012)
Upgrading and downgrading of prostate cancer from biopsy to radical prostatectomy: evidence and protective factory using the modifical Gleason grading
Eur. Urol. 61 1019-24Kristiansen, G.; Egevad, L.; Amin, M. et al.
Konsensuskonferenz 2014 der ISUP zur Gleason-Graduierung des Prostatakarzinoms
Pathologe DO/10.1007/s 00292-015-0136-6
published online 26.1.2016Helpap, B et al. (2007) The value of the modified Gleason grading system of prostate adenocarcinoma in routine urological diagnostics Urologe 2007 Jan; 46(1): 59-62.
Leitlinienprogramm Onkologie
(Deutsche Krebsgesellschaft, Deutsche Krebshilfe AWMF) : Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms. Langversion 5.0, 2018 AWMF Registernummer 043/022 OLMottet, N. et al.: Guidelines on prostate cancer. European Association of Urology (EAU) 2018. Neueste Version verfügbar auf der EAU-Website über die Seite der onkologischen Leitlinien als PDF (englisch)
Rübben, H. (Hrsg.): Uroonkologie. 6. Auflage, Springer Medizin Verlag, Heidelberg 2014