Hormontherapie
Das Prostatakarzinom steht mit ca. 65.000 Neuerkrankungen/Jahr in Deutschland an erster Stelle der soliden bösartigen Erkrankungen (Robert-Koch-Institut Berlin 2017). Die verbesserte Diagnostik hat nicht zuletzt dazu beigetragen, dass heutzutage die meisten Prostatakarzinome in einem frühen, organbegrenzten Stadium entdeckt werden und damit kurativ behandelt werden, d. h., die Patienten geheilt werden können.
Dennoch ist in den letzten Jahren eine Stadienverschiebung eingetreten zu aggressiveren, lokal und systemisch fortgeschrittenen Prostatakarzinomen.
Bei fortgeschrittenem Prostatakrebs kann eine der vielen Formen des Androgenentzugs helfen. Er erfolgt meist medikamentös mit einem LH-RH-Analogon, manchmal in Kombination mit einem Antiandrogen.
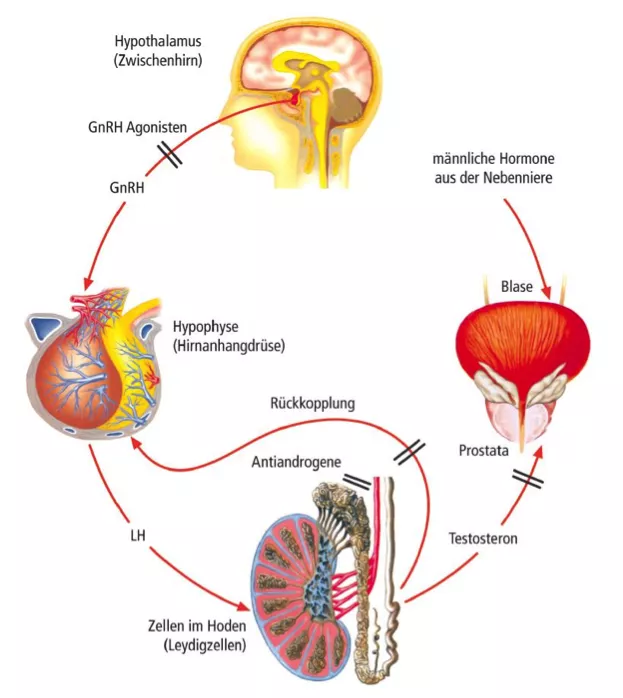
Das Wachstum und die Funktion normaler Prostatazellen sind abhängig von Androgenen (männlichen Geschlechtshormonen). Die Androgene, deren Hauptvertreter das Testosteron ist, werden zum größten Teil in den Hoden unter dem Einfluss des Hormons LH gebildet. Ein kleiner Teil stammt auch aus den Nebennieren (Näheres zu allen Hormonen und ihrer Regulation im nächsten Bild und unter Sexualhormone).
Auch für das Wachstum bösartiger Prostatazellen spielen Androgene eine wichtige Rolle (s. Abschnitt Ursachen). Dass ihre künstliche Absenkung bei fortgeschrittenem Prostatakrebs wirksam ist, wurde 1941 erstmals beschrieben, und Charles Huggins bekam später den Nobelpreis für diese Entdeckung. Zu erreichen ist das Ziel auf zwei Wegen, die man beide als Androgenentzug (oder ADT = Androgendeprivationstherapie) bezeichnet: Entweder durch Absenken der Androgenproduktion mittels Orchiektomie (Entfernung der Hoden), LH-RH-Analoga, LH-RH-Antagonisten und Östrogenen, oder aber durch Hemmung der Androgenwirkung mit Antiandrogenen (siehe nächste Abschnitte).
Eingesetzt wird die Hormontherapie hauptsächlich bei fortgeschrittenem Prostatakrebs (Näheres dazu siehe unten). Dabei hat sie folgende Wirkungen: Sie verzögert die Zeit bis zum Fortschreiten der Erkrankung, verhindert schwere Komplikationen des Tumors und lindert die Beschwerden. Zunächst zu den verschiedenen Methoden des Androgenentzugs:
Bilaterale Orchiektomie
Hierunter versteht man die Entfernung beider Hoden, die chirurgische Kastration. Sie ist die älteste Form der Hormontherapie und wird heute nur noch selten durchgeführt, meist als subkapsuläre Orchiektomie, als Ausschälung des Androgen-produzierenden Gewebes unter Belassung von Hodenhüllen und Nebenhoden. Dadurch sinkt der Testosteron-Blutspiegel auf das so genannte Kastrationsniveau von weniger als 50 ng/dl.
Vorzüge sind die geringen Kosten, der relativ einfache Eingriff, die rasche und dauerhafte Hormonsenkung sowie die geringe Notwendigkeit häufiger Arztbesuche. Als Nachteile gelten die im Vergleich zum medikamentösen Androgenentzug (s. nächste Abschnitte) größere psychische Belastung, die Tatsache, dass der Eingriff irreversibel, das heißt nicht rückgängig zu machen ist, sowie mögliche Komplikationen des operativen Eingriffs. Er kommt deshalb heute nur noch in Sonderfällen zum Einsatz (z.B. zur raschen Linderung von Schmerzen durch Metastasen). Zu den Nebenwirkungen s. Androgenentzugssyndrom.
LH-RH-Analoga
LH-RH-Analoga sind Medikamente, die ebenso wirken wie LH-RH (analog zu diesem), weshalb man sie auch LH-RH-Agonisten (Wettbewerber) nennt. Ihre kontinuierliche Anwendung führt zunächst zu einer Ausschüttung von LH aus der Hypophyse und damit zu einem Anstieg des Androgenspiegels (flare-up-Phänomen, nach 2-3 Tagen für etwa 7 Tage; vgl. Abbildung oben, GnRH andere Bezeichnung für LH-RH). Wegen der Dauerstimulation der Hypophyse kommt es dann jedoch zur so genannten medikamentösen Kastration: Die LH-RH-Rezeptorenzahl der Hypophyse nimmt ab, so dass sie gegen LH-RH unempfindlich wird, die Freisetzung von LH abfällt und der Androgenspiegel nach 2-4 Wochen auf Kastrationsniveau sinkt (Testosteron weniger als 50 ng/dl).
Die Wirkstoffe werden in Form von Depots unter die Haut oder in die Muskulatur injiziert. Die jeweiligen Präparate weisen ähnliche oder gleiche Wirkqualitäten auf. Sie unterscheiden sich jedoch in der Wirkdauer des Depots (ein, zwei, drei oder sechs Monate) und damit in der Zahl der pro Jahr nötigen Injektions-Spritzen. Daneben gibt es Unterschiede in der Darreichungsform (z. B. flüssige Suspension oder festes Stäbchen = Implantat), die die Dicke der zum Injizieren nötigen Injektions-Nadel bestimmt. Wegen des anfänglichen Androgenanstiegs kann in den ersten 2-4 Wochen zusätzlich ein Antiandrogen (s. unten) gegeben werden, vor allem bei weit fortgeschrittenen Tumoren.
Die Behandlung mit LH-RH-Analoga gilt heute als Standard bei allen Formen der Hormontherapie. Sie ist gleich wirksam wie die Orchiektomie, im Gegensatz zu dieser jedoch reversibel (rückgängig zu machen), das heißt nach Absetzen der LH-RH-Analoga wird die Androgenproduktion bei den meisten Männern wieder angeregt. Zusätzlich entfällt die mit der Entfernung der Hoden verbundene psychische Belastung. Ansonsten sind die möglichen Nebenwirkungen vergleichbar (s. unten).
LH-RH-Antagonisten
Diese Medikamente sind die „Gegenspieler“ des natürlichen LH-RH: Sie blockieren dessen Rezeptoren an der Hypophyse (vgl. Abbildung oben). In Studien mit bis zu 5 Jahren Beobachtungsdauer haben sie die gleiche Wirksamkeit in Bezug auf Testosteronsenkung gezeigt wie die LH-RH-Agonisten. Im Unterschied zu diesen verursachen sie keinen anfänglichen Androgenanstieg und dadurch einen schnelleren Abfall der Androgene auf Kastrationsniveau. Sie sind nur als 1-Monats-Depot verfügbar, wohingegen die LH-RH-Agonisten als 1-, 2-, 3- und 6-Monats-Depots verfügbar sind und seit mehr als 25 Jahren in der Behandlung des Prostatakarzinoms erfolgreich eingesetzt werden. Beide Substanzklassen unterscheiden sich im jeweiligen Nebenwirkungsprofil (allgemeine Nebenwirkungen, siehe unten „Androgenentzugssyndrom“).
Östrogene
Östrogene (weibliche Geschlechtshormone) werden in geringer Menge auch beim Mann gebildet und sind für seinen Körper sehr wichtig (s. auch Sexualhormone). In höherer Dosis zur Behandlung eingesetzt, wirken sie über verschiedene Mechanismen, unter anderem über eine Hemmung der LH-RH-Freisetzung, und führen zu einer Senkung des Androgenspiegels auf Kastrationsniveau nach 3-9 Wochen (vgl. Abbildung oben). Sie waren historisch zunächst die erste Möglichkeit der medikamentösen Kastration als Ersatz für die Orchiektomie und erwiesen sich als gleichwirksam. Neben den erwarteten Nebenwirkungen (s. unten) traten jedoch dosisabhängig auch vermehrt solche des Herz-Kreislauf-Systems auf, so dass man Östrogene allein heute kaum noch verwendet.
Antiandrogene
Alle Antiandrogene blockieren die Rezeptoren der Androgene an den Zielzellen und verhindern so deren Wirkungen (vgl. Abbildung oben). Diese Substanzen werden als Tabletten verabreicht und nach ihrer Struktur in steroidale und nicht steroidale Antiandrogene unterteilt:
Steroidale Antiandrogene:
Die Wirkstoffe enthalten ein so genanntes Steroid-Grundgerüst. Sie blockieren die Wirkung der Androgene und senken zusätzlich deren Blutspiegel, indem sie die LH-Freisetzung aus der Hypophyse hemmen. Von den verfügbaren Wirkstoffen ist das Cyproteronacetat (CPA) am besten untersucht: Der Androgenspiegel fällt rasch auf etwa ein Viertel des Ausgangswertes, aber nicht auf Kastrationsniveau. Dennoch sind die Nebenwirkungen ähnlich wie bei der Orchiektomie (s. unten), wobei Libidoverlust und erektile Dysfunktion häufig auftreten, die Gynäkomastie dagegen tritt nur selten auf. CPA alleine scheint schwächer wirksam zu sein als LH-RH-Analoga und Orchiektomie, aber ähnlich wie nicht steroidale Antiandrogene (s. nächster Absatz). Eingesetzt wird es vor allem zu Beginn einer LH-RH-Analoga-Therapie (wegen des anfänglichen Androgenanstiegs, s. oben) sowie – in geringerer Dosis – zur Verhinderung von Hitzewallungen bei anderweitiger Hormontherapie.
Nicht steroidale Antiandrogene:
Sie blockieren nur die Wirkung der Androgene. Betroffen ist auch jene am Gehirn, die normalerweise dafür sorgt, dass weniger LH ausgeschüttet und damit die Produktion der Androgene gebremst wird (s. auch Sexualhormone). Der Androgenspiegel kann deshalb leicht steigen, bleibt aber meist gleich. Die Nebenwirkungen unterscheiden sich von denen der Orchiektomie und der anderen Medikamente (s. nächster Absatz): Libido, Erektion, körperliche Leistung und Knochendichte werden meist nicht so stark beeinträchtigt. Häufig kommt es aber zu Schmerzen und Vergrößerungen der Brustdrüse. Die vorbeugende Bestrahlung der Brustdrüsen (Mammillen-Bestrahlung) gilt hier als wirksame Therapie. Weitere Nebenwirkungen hängen vom Wirkstoff ab. Verwendet werden diese Medikamente als Monotherapie, bei der maximalen Androgenblockade (beide s. nächste Absätze) sowie zu Beginn einer Therapie mit LH-RH-Analoga (s. oben).
Neuere Medikamente beim metastasierten kastrationsresistenten Prostatakarzinom (mCRPC)
Zur Behandlung des kastrationsresistenten Prostatakarzinoms (CRPC, Näheres s. unten) gibt es zwei neuere Medikamente, die in Kombination mit LH-RH-Analoga eingesetzt werden sollen: Abirateron blockiert die Bildung von Androgenen (männlichen Geschlechtshormonen) und von Östrogenen (weiblichen Geschlechtshormonen). Dies betrifft den gesamten Körper, also die Hoden, die Nebennieren und auch die Prostatakrebszellen. Abirateron muss mit einem Kortikosteroid (z. B. Prednison) kombiniert werden. Bei der Behandlung können zahlreiche Nebenwirkungen auftreten. Enzalutamid ist ein neuartiges nicht steroidales Antiandrogen (der „3. Generation“). Es unterscheidet sich von den bislang verfügbaren Wirkstoffen (s. oben) sowohl bezüglich der Wirkungsweise als auch bezüglich möglicher Nebenwirkungen.
Androgen-Entzugssyndrom
Es ist definiert durch eine aktivierende Wirkung von Antiandrogenen bei mutierten (genetisch veränderten) Androgenrezeptoren.
Unter diesem Begriff fasst man die Nebenwirkungen der Hormonsenkung zusammen. Je nach Methode und Wirkstoff können verschiedene unerwünschte Wirkungen auftreten (s. auch in den vorherigen Absätzen). Über die häufigsten und ihre Behandlungsmöglichkeiten muss der Patient eingehend aufgeklärt werden:
- Hitzewallungen (engl. hot flush, hot flash) und Schweißausbrüche. Behandlung: Medikamente (z. B. Cyproteronacetat, ein Antiandrogen, s. auch oben)
- Verlust der Libido („sexuelle Lust“)
- Erektionsstörungen. Behandlung s. erektile Dysfunktion
- Schmerzen und Vergrößerung (Gynäkomastie) der Brustdrüsen (hauptsächlich bei der Therapie mit Antiandrogenen, s. oben). Behandlung: Vorbeugende Mammillen-Bestrahlung, Operation, evtl. Medikamente
- Gewichtszunahme, Muskelabbau, Veränderungen des Stoffwechsels; diese Nebenwirkungen können das Risiko für Herz-Kreislauf-Erkrankungen und Diabetes mellitus (Zuckerkrankheit) erhöhen. Behandlung: Bewegung, Muskeltraining, Ernährungsumstellung
- Blutarmut (Anämie); kann unter anderem zu Schwäche, Müdigkeit und Luftnot führen. Behandlung: Bluttransfusion, evtl. Medikamente
- Knochenabbau (Osteoporose); erhöht das Risiko für Knochenbrüche. Behandlung: Bewegung, Training, Kalzium, Vitamin D, Medikamente
Umfang und Art des Androgen-Entzugs
Monotherapie: Anwendung nur eines Verfahrens (Monotherapie), meist als kontinuierlicher Androgenentzug mit einem LH-RH-Analogon, seltener mittels Orchiektomie, LH-RH-Antagonisten oder eines nicht steroidalen Antiandrogens. Wegen der Nebenwirkungen, auch bezüglich der Sexualfunktion, wurden andere Behandlungsmöglichkeiten untersucht, wie z.B. der intermittierende und aufgeschobene Androgenentzug (s. nächste Absätze).
Maximale Androgenblockade (MAB): Diese bezeichnet man auch als komplette Androgenblockade (engl. complete androgen blockade, CAB). Dabei wird nicht nur die Androgenproduktion in den Hoden ausgeschaltet, sondern auch die Wirkung der restlichen, in den Nebennieren gebildeten Androgene blockiert (5-10 %, s. auch Sexualhormone). In der Regel beinhaltet die MAB eine Kombination aus einem LH-RH-Analogon und einem nicht steroidalen Antiandrogen. Studien sprechen dafür, dass bei der MAB mehr Nebenwirkungen auftreten als bei der Monotherapie, so dass sie nur selten zum Einsatz kommt, nicht zuletzt wegen einer erheblichen Beeinträchtigung der Lebensqualität (Sexualität, kognitive Funktion, Hitzewallungen).
Kontinuierlicher oder intermittierender Androgenentzug? Die Wirkung des kontinuierlichen Androgenentzugs (engl. continuous androgen deprivation, CAD) lässt mit der Zeit nach, der Tumor wird Androgen-unabhängig (s. unten). Der intermittierende (zeitweise unterbrochene) Androgenentzug (engl. intermittent androgen deprivation, IAD), der naturgemäß nach einer Orchiektomie nicht möglich ist, hat zum Ziel, diese Zeit zu verlängern und zugleich die Nebenwirkungen (z. B. auf die Sexualfunktion) zu vermindern. Dazu legt man eine untere und eine obere Grenze für den PSA-Wert fest und führt den Androgenentzug nur so lange durch, bis der PSA-Wert die untere Grenze erreicht hat. Sollte der Wert wieder ansteigen und die obere Grenze überschreiten, wird die Therapie fortgeführt. Damit bleibt im Schnitt die Hälfte der Zeit therapiefrei, in der der Androgenspiegel wieder ansteigt, die Nebenwirkungen gehen zurück und die Lebensqualität steigt. Derzeit gilt der intermittierende Androgenentzug als ähnlich wirksam wie der kontinuierliche. Einige wichtige Fragen sind im Detail noch ungeklärt, und es liegen nur wenige valide Langzeitdaten vor (z. B. zur Überlebenszeit). Wird eine intermittierende Androgen-Blockade (Androgen-Deprivation) angestrebt, ist der Patient auch darüber aufzuklären, dass nach neuesten internationalen wissenschaftlichen Studien ein wahrscheinlich um 20 % höheres Sterberisiko im Vergleich zur kontinuierlichen Hormonbehandlung besteht.
Sofortiger oder aufgeschobener Androgenentzug: Der optimale Zeitpunkt zum Beginn einer Hormontherapie ist bislang noch nicht in allen Fällen klar. So stellt sich die Frage, ob diese bei einem Patienten mit Prostatakrebs, der noch keine Krankheitszeichen verursacht, gefahrlos aufgeschoben werden kann, um die Nebenwirkungen der Therapie vorerst zu vermeiden.
Hormontherapie beim nicht metastasierten Prostatakarzinom
Bei Prostatakrebs ohne Metastasen (Tochtergeschwülste) spricht man je nach dessen örtlicher Ausdehnung von einem lokal begrenzten oder von einem lokal fortgeschrittenen Prostatakarzinom (T1-2 N0 M0 bzw. T3-4 N0 M0, zum TNM-System s. Abschnitt Wachstum und Ausbreitung). Hier empfiehlt sich eine kurative (auf Heilung zielende) Behandlung (aktive Überwachung, radikale Prostatektomie oder Strahlentherapie; s. dazu auch den Abschnitt Behandlungsplanung). Zur Hormontherapie im Zusammenhang mit der Operation siehe Abschnitt „Radikale Prostatektomie“ unter adjuvante Therapie. Zur Hormontherapie im Zusammenhang mit der Strahlentherapie siehe dort unter lokal begrenztes Prostatakarzinom und lokal fortgeschrittenes Prostatakarzinom.
Entscheidet sich ein Patient mit einem lokal begrenzten oder lokal fortgeschrittenen Prostatakarzinom nicht für eine kurative, sondern für eine palliative (lindernde) Therapie, kann man nach ausführlicher Aufklärung sofort eine Hormontherapie einleiten oder ihn zunächst abwartend beobachten (Näheres zur Aufklärung und Entscheidungsfindung s. Abschnitt abwartendes Beobachten).
Lehnt ein Patient mit einem lokal begrenzten Prostatakarzinom eine kurative Therapie ab, kann ihm nach ausführlicher Aufklärung auch eine Hormontherapie angeboten werden. Soll ein Patient mit einem lokal fortgeschrittenen Tumor eine solche Therapie erhalten, kann er mittels chirurgischer oder medikamentöser Kastration (z. B. LH-RH-Analogon, LH-RH-Antagonist, in seltenen Fällen mit bilateraler Orchiektomie - alle s. o.) oder mit einem Antiandrogen (z. B. Bicalutamid 150 mg pro Tag) behandelt werden. Die hormonablative Therapie ist beim lokalen biochemischen Rezidiv (PSA-Rezidiv) oder bei PSA-Progression keine Standard-Therapie.
Hormontherapie beim metastasierten Prostatakarzinom
Von einem metastasierten Prostatakarzinom spricht man, wenn die regionären (örtlichen) Lymphknoten befallen sind (N1) oder wenn Metastasen (Tochtergeschwülste) in entfernten Lymphknoten oder an anderen Stellen des Körpers vorhanden sind (M1; zum TNM-System s. Abschnitt Wachstum und Ausbreitung).
Ein Lymphknotenbefall lässt sich bei der radikalen Prostatektomie oder in einem separaten Eingriff durch eine Lymphadenektomie (Entnahme) mit anschließender histologischer (feingeweblicher) Untersuchung nachweisen. Ist dies der Fall und liegen keine weiteren Metastasen vor (pN1 M0), kommen als lokale Behandlung des Tumors die radikale Prostatektomie oder die Strahlentherapie infrage und als systemische (allgemeine) Behandlung die sofortige oder aufgeschobene Hormontherapie (s. dazu auch den Abschnitt „Behandlungsplanung“ unter Lymphknotenbefall). Die Entscheidung ist individuell zu treffen, weil es derzeit keinen verlässlichen Vergleich dieser Verfahren gibt, weder allein noch in Kombination. Gleiches gilt, wenn eine Lymphknoten-Entnahme nicht möglich ist und das Befallsrisiko als hoch eingeschätzt wird. Bei einem bereits klinisch erkennbaren Lymphknotenbefall (cN1, z. B. mit bildgebenden Verfahren) ist mit Metastasen auch an anderen Stellen zu rechnen (M1, s. u.). Mehr zur Hormontherapie beim Lymphknotenbefall ohne weitere Metastasen siehe Abschnitt „Radikale Prostatektomie“ unter adjuvante Therapie und Abschnitt „Strahlentherapie“ unter Lymphknotenbefall.
Bei einem Rezidiv (Wiederauftreten) des Prostatakarzinoms nach kurativer (auf Heilung zielender) Erstbehandlung kann auch eine Hormontherapie infrage kommen. Siehe hierzu die Abschnitte „Behandlungsplanung“ unter rezidiviertes Prostatakarzinom, „Radikale Prostatektomie“ unter Rezidivtherapie sowie „Strahlentherapie“ unter Rezidivtherapie.
Bei einem metastasierten Prostatakarzinom sollen die Patienten über die Hormontherapie aufgeklärt werden, vor allem darüber, dass sie palliativ (lindernd) ist, dass sie die Lebensqualität beeinträchtigen kann, welche unerwünschten Wirkungen möglich sind und dass bei sofortiger Therapie sich zwar die Zeit bis zum Fortschreiten des Tumors (das progressionsfreie Überleben) verlängert, aber noch unklar ist, ob dies auch für die Zeit bis zum Tod (das Gesamtüberleben) gilt. So stellen sich im metastasierten Stadium Fragen, womit und wie lange (kontinuierlich oder intermittierend) die Hormontherapie erfolgen soll. Die Geschwindigkeit sowie der Umfang des Ansprechens einer Hormonbehandlung sind gegenwärtig die besten Kriterien, um die Dauer des Therapieerfolges abzuschätzen. Die Möglichkeiten der kombinierten Hormontherapie mit Docetaxel oder mit Abirateron (plus Prednison/Prednisolon) haben die Erstlinienbehandlung des metastasierten hormonsensitiven Prostatakarzinoms bei Erstdiagnose grundlegend verändert.
Patienten, die bereits Symptome (Krankheitszeichen) haben, soll dann eine sofortige Hormontherapie empfohlen werden, Patienten ohne Symptome kann die (sofortige oder aufgeschobene) Hormontherapie angeboten werden (s. hierzu auch den Abschnitt „Behandlungsplanung“ unter Fernmetastasen). Ist ein Androgenentzug angezeigt, soll er mit Medikamenten (LH-RH-Analoga, LH-RH-Antagonisten, keine Monotherapie mit steroidalen Antiandrogenen; alle s. oben)oder operativ (mit bilateraler Orchiektomie s. o.) erfolgen.
Alternativ kann Patienten mit metastasiertem Prostatakrebs eine Therapie mit einem nicht steroidalen Antiandrogen angeboten werden (s. oben) kann als Erstbehandlung zum Einsatz kommen. Studien weisen auf einen nur kleinen Überlebensvorteil im Vergleich zur Monotherapie zwecks Hormonsenkung hin, jedoch bei vermehrten Nebenwirkungen. Ebenso kann nach entsprechender Aufklärung ein intermittierender Androgenentzug (IAD, s. oben) empfohlen werden.
Bestandteil der umfänglichen Aufklärung über eine alleinige Hormonbehandlung (Androgendeprivation=ADP) oder eine Kombinationstherapie mit z. B. Docetaxel muss schwerpunktmäßig folgende Eckdaten enthalten: Hinweis auf palliativen Charakter der Therapie, Einfluss auf die Lebensqualität und die auftretenden unerwünschten Nebenwirkungen der Therapie.
Fortschreitender Prostatakrebs unter Hormontherapie
Der Prostatakrebs spricht in den meisten Fällen (80-90%) zunächst auf die Hormontherapie an, erkennbar an einer Besserung der Beschwerden, einer Verkleinerung des Tumors und dem Abfall des PSA-Wertes und des Testosteron-Blutspiegels (auf Kastrationsniveau von weniger als 50 ng/dl). Aus noch nicht eindeutig geklärten Gründen schreitet er trotzdem nach einigen Jahren fort, was sich am Wiederanstieg des PSA-Werts oder an Krankheitszeichen, meist Knochenschmerzen (durch Metastasen), zeigt.
Obwohl der Tumor zuvor nicht immer vollständig beseitigt war, spricht man hier dennoch von einem Rezidiv (Wiederauftreten der Erkrankung), und zwar bei einem PSA-Wiederanstieg von einem biochemischen Rezidiv (BCR, Labor-Zeichen für ein Wiederauftreten), beim Weiterwachsen am ursprünglichen Ort von einem Lokalrezidiv (Tumorrezidiv) und beim Wachstum von Metastasen in Lymphknoten oder an anderen Stellen des Körpers von einem systemischen Rezidiv.
Weil der Tumor bei unterdrücktem Androgenspiegel fortschreitet, nennt man ihn Androgen-unabhängiges oder kastrationsresistentes Prostatakarzinom. Dennoch reagiert er meist noch auf Änderungen des Androgenentzugs und die Gabe anderer hormonwirksamer Medikamente.
Spricht der Tumor nicht mehr auf diese Maßnahmen an, gilt er als kastrationsresistentes Prostatakarzinom (CRPC, früher auch hormonrefraktäres = Hormon-unempfindliches Prostatakarzinom, HRPC). Es sollte nur so genannt werden, wenn der Testosteron-Blutspiegel auf Kastrationsniveau liegt (weniger als 50 ng/dl), wenn der PSA-Wert dreimal in Folge im Abstand von jeweils einer Woche angestiegen ist, wobei zwei Werte mindestens 50 % über dem Nadir (Tiefpunkt) liegen müssen und der Höchstwert über 2 ng/ml beträgt, wenn das Antiandrogen für mindestens 4 Wochen abgesetzt oder ein anderes hormonwirksames Medikament gegeben wurde und wenn mindestens zwei Metastasen neu aufgetreten sind oder sich vergrößert haben.
Behandlung bei fortschreitendem Prostatakrebs unter Hormonsenkung: Zuerst soll der Testosteron-Spiegel kontrolliert werden, um zu prüfen, ob die bisherige Behandlung die Androgene ausreichend unterdrückt hat und der Tumor tatsächlich Androgen-unabhängig ist. Dann soll der Patient darüber aufgeklärt werden, dass eine Heilung nicht möglich ist, eine sekundäre Hormonmanipulation (s.o.) oder eine zusätzliche Chemotherapie die Beschwerden lindern kann, eine Chemotherapie oder eine Zweitlinientherapie mit Abirateron oder Enzalutamid (beide s. Abschnitt Chemotherapie) die Überlebenszeit im Schnitt um einige Monate verlängert, die Behandlungen Nebenwirkungen haben können und die Auswirkungen auf die Lebensqualität unzureichend untersucht sind. Bei der Therapieentscheidung sollen bedacht werden: Beschwerden, Begleiterkrankungen, Lebenserwartung, Lebensqualität und – nicht zuletzt - Wünsche des Betroffenen, Nebenwirkungen der einzelnen Therapien, Geschwindigkeit des Fortschreitens des Tumors sowie Lokalisation von Metastasen und Tumorlast (Krebsmenge).
Erstlinientherapie bei Patienten ohne Beschwerden: Man kann dem Patienten das Abwarten unter dem bisherigen Androgen-Entzug (s. o.) anbieten. Wie sich das Absetzen des Androgen-Entzugs auswirkt, ist noch nicht ausreichend untersucht. Der Patient soll vor der Entscheidung darüber aufgeklärt werden, dass es sich um palliative (lindernde) Behandlungen handelt, dass eine maximale Androgenblockade (s. oben) zusätzliche Nebenwirkungen hat. Man kann ihm eine Chemotherapie oder Abirateron bzw. Enzalutamid anbieten, wenn der PSA-Wert rasch ansteigt (Verdopplungszeit = PSA-DT unter 3 Monaten), wenn das Fortschreiten mit bildgebenden Verfahren nachgewiesen wurde oder wenn der Patient bei steigendem PSA-Wert diese Behandlung wünscht. Es ist jedoch nicht erwiesen, dass eine frühe Chemotherapie, die beginnt, solange noch keine Beschwerden vorliegen, ein längeres Überleben zur Folge hat, als wenn man sie erst bei Symptomen einleitet (Weiteres s. Abschnitt Chemotherapie).
Erstlinientherapie bei Patienten mit Beschwerden: Die Behandlungsmöglichkeiten und das weitere Vorgehen sollen von Ärzten aller betroffenen Fachdisziplinen (z. B. in einem interdisziplinären Tumorboard) besprochen und festgelegt werden. Der Patient soll vor der Entscheidung darüber aufgeklärt werden, dass es sich um eine palliative (lindernde) Behandlung handelt, die Therapien nur bei einem Teil der Patienten zu einer Linderung der Beschwerden oder einer Lebensverlängerung führen und eine Chemotherapie mehr Nebenwirkungen hat als eine Hormontherapie oder die Gabe von Kortikosteroiden. Wichtig ist, dass bei Kastrationsresistenz die medikamentöse Kastration (Hormontherapie) fortgesetzt werden sollte, da gegenwärtig über deren eventuelle Beendigung keine validen wissenschaftlichen Daten bestehen.
Je nach Befund kann man anbieten:
- Hormontherapie (bis hin zu Abirateron, Enzalutamid)
- Gabe von Kortikosteroiden (s. o.)
- Chemotherapie
- Behandlung von Krankheitszeichen (Supportivtherapie, s. Abschnitt Palliativmedizin)
- Behandlung von Knochenmetastasen (s. Abschnitt Palliativmedizin)
Bei Patienten mit einem metastasierten kastrationsresistenten Prostatakarzinom, bei denen der Androgenentzug versagt hat, eine Chemotherapie aber noch nicht angezeigt ist, und die keine oder nur milde Beschwerden haben, ist eine Behandlung mit Abirateron (ein Hemmstoff für die Bildung von Androgenen und Östrogenen) oder Enzalutamid sinnvoll. Abirateron in Kombination mit Prednison oder Prednisolon ist zur täglichen Einnahme beim kastrationsresistenten Prostatakarzinom sowohl in der Erstlinientherapie als auch nach Chemotherapie (z. B. mit Docetaxel) zugelassen.
Ebenso bietet sich der Einsatz von Enzalutamid bei guter Wirksamkeit und Verträglichkeit sowohl vor als auch nach einer Chemotherapie (z. B. mit Docetaxel) als sehr gute Therapiemöglichkeit an.
Neue Substanzen
Abirateron
Diese Substanz hemmt ein Enzym, das für die Androgenbiosynthese in den Hoden, den Nebennieren und der Prostata vorkommt und unterdrückt somit die Androgenproduktion auch außerhalb der Gonaden. In Verbindung mit einer Androgendeprivationstherapie findet es nicht nur beim kastrationsrefraktären Prostatakrebs nach einer Chemotherapie mit Docetaxel Anwendung, sondern auch bei noch nicht chemotherapierten Patienten mit metastasiertem Prostatakarzinom. Wegen seiner Wirksamkeit bei diesen Hochrisikopatienten kommt es zunehmend zum Einsatz. Die Kombination mit Prednison oder Prednisolon, das gegen den eventuellen Anstieg der Mineralkortikoide wirkt, ist dabei erforderlich.
Enzalutamid
Diese Substanz wird oral eingenommen und agiert u. a. als Antagonist des Androgen-Rezeptors (AR), hemmt die Verlagerung des AR-Komplexes in den Zellkern und die damit verbundenen Signalübertragungswege.
Enzalutamid verbesserte in einer klinischen Studie mit Patienten, die ein kastrationsresistentes, asymptomatisches bis mild symptomatisches, metastasiertes Prostatakarzinom hatten und zuvor noch keine Chemotherapie erhielten, gegenüber Placebo sowohl das Gesamtüberleben als auch das radiologische progressionsfreie Überleben. Im Vordergrund der therapiebegleitenden Nebenwirkungen standen Fatigue (Müdigkeit) und Rückenschmerzen bei insgesamt minimalen Nebenwirkungen.
Enzalutamid wurde auch sehr erfolgreich beim Fortschreiten der metastasierten, kastrationsresistenten Prostatakrebserkrankung nach einer Chemotherapie eingesetzt. In der bei diesen Patienten durchgeführten Studie verbesserte Enzalutamid gegenüber Placebo sowohl das Gesamtüberleben als auch das radiologische progressionsfreie Überleben.
Beer TM, Armstrong AJ, Rathkopf DE, et al. Enzalutamide in metastatic prostate cancer before chemotherapy. N Engl J Med. 2014;371:424–33.
James ND, de Bono JS, Spears MR et al. Abiraterone for Prostate Cancer Not Previously Treated with Hormone Therapy. N Engl J Med 2017; 377: 338–351
Leitlinienprogramm Onkologie
(Deutsche Krebsgesellschaft, Deutsche Krebshilfe AWMF) : Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms. Langversion 5.0, 2018 AWMF Registernummer 043/022 OLMichel, M. St.; Thüroff, W. J.; Janetschek, G.; Wirth, M. (Hrsg.)
Die Urologie
Springer-Verlag Berlin Heidelberg 2016Mottet, N. et al.: Guidelines on prostate cancer. European Association of Urology (EAU) 2018. Neueste Version verfügbar auf der EAU-Website über die Seite der onkologischen Leitlinien als PDF (englisch)
Ryan CJ, Smith MR, de Bono JS et al. Abiraterone in metastatic prostate cancer without previous chemotherapy. N Engl J Med 2013; 368: 138–148
Robert Koch Institut (Hrsg.): Krebs in Deutschland 2013/2014. 11. Ausgabe, Berlin 2017.
Neueste Version verfügbar als PDF auf der RKI-Website (unter Gesundheitsmonitoring - Krebsregisterdaten)Rohayem, J., et al.: Antiandrogene Therapie des Prostatakarzinoms. Indikation und systemische Folgen. CME Zertifizierte Fortbildung. Urologe 2012; 51: 557-566
Rübben, H. (Hrsg.): Uroonkologie. 7. Auflage, Springer Medizin Verlag, Heidelberg 2014, ISBN 978-3-540-33847-5
Scher HI, Fizazi K, Saad F et al. Increased survival with enzalutamide in prostate cancer after chemotherapy. N Engl J Med 2012; 367: 1187–1197
Thelen, P., et al.: Intermittierende Hormontherapie beim androgensensiblen Prostatakarzinom. Sinn oder Unsinn? Urologe 2012; 51: 1240-1245, DOI 10.1007/s00120-012-2870-1
Die Radikaloperation der Prostata beim Prostatakarzinom – Ein Leitfaden für Patienten, 8. Auflage